POLYARTHRITE RHUMATOÏDE
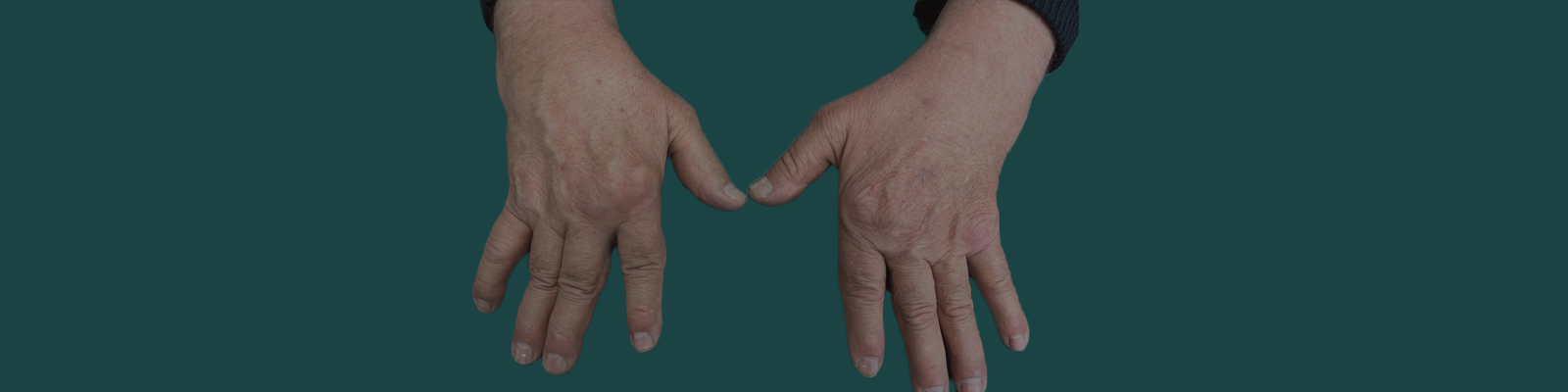
Qu'est-ce qu'une polyarthrite rhumatoïde ?
La polyarthrite rhumatoïde (PR) fait partie de la famille des « rhumatismes inflammatoires chroniques » ou «RIC». Elle se manifeste par des poussées douloureuses et des gonflements des articulations.
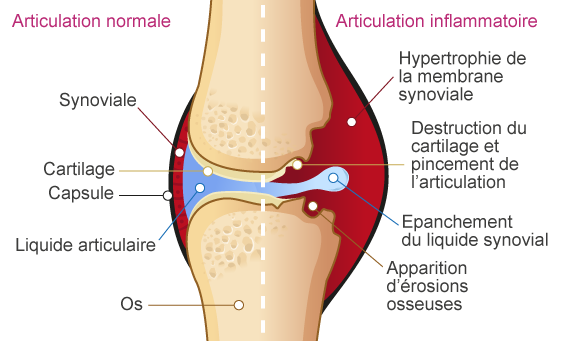
Dans la PR, l’inflammation est due à un dérèglement de l’immunité : le système inflammatoire est stimulé en permanence. Il en résulte une inflammation qui persiste dans le temps, devient chronique et devient alors néfaste pour les articulations.
Cette inflammation peut, à terme, créer des lésions aux articulations.
Qui est touché par la Polyarthrite Rhumatoïde ?
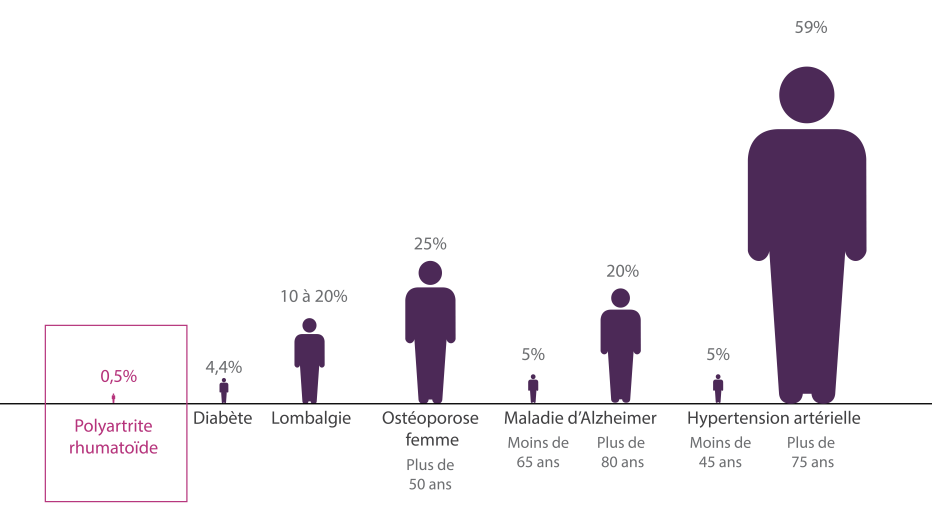
La PR est le rhumatisme inflammatoire le plus fréquent ; elle touche environ 0,5 % de la population, le plus souvent des femmes de plus de 50 ans (quatre femmes pour un homme).
Quelles sont les causes de la Polyarthrite Rhumatoïde ?
La PR est une maladie auto-immune dont l’origine exacte reste encore inconnue.
Plusieurs facteurs peuvent intervenir pour dérégler le fonctionnement du système immunitaire et favoriser la survenue d’une PR. Le degré d’implication de ces différents facteurs dans la survenue de la PR n’est pas connu avec certitude et fait l’objet de recherches.
Les facteurs environnementaux peuvent influencer la survenue de la maladie.
Le tabac joue un rôle important car il favorise le déclenchement de la PR d’autant plus que les personnes sont prédisposées d’un point de vue génétique et ont une consommation tabagique élevée.
Les facteurs hormonaux jouent un rôle dans la maladie, car la PR atteint surtout les femmes.
On a aussi constaté que même si la PR peut atteindre des personnes jeunes, la PR survient habituellement au moment de la ménopause. Il existe souvent une rémission de la maladie pendant la grossesse alors qu’une poussée est possible au cours de l’accouchement ou pendant l’allaitement.
Néanmoins, d’autres facteurs hormonaux peuvent intervenir.
La PR n’est pas une maladie héréditaire mais une maladie à prédisposition génétique.
Cela signifie que les facteurs génétiques jouent un rôle, mais que celui-ci reste relativement faible, expliquant environ un tiers du déclenchement de la maladie. Le terrain génétique justifie l’existence de familles dans lesquelles plusieurs personnes sont atteintes.
À l’inverse, certaines personnes porteuses de cette prédisposition génétique ne développeront pas la PR. Cela suggère que des gènes non encore identifiés pourraient être impliqués et qu’il est nécessaire qu’interviennent d’autres facteurs pour déclencher la maladie.
Par conséquent, il n’existe pas de dépistage génétique de la PR, ni chez les personnes atteintes ni chez leurs enfants.
Les facteurs infectieux sont de plus en plus incriminés,notamment certaines bactéries telles que Porphyromonas gingivalis. Elles sont responsables d’infections dentaires chez des personnes ayant une hygiène ou des soins dentaires insuffisants, ou souffrant de parodontite (inflammation chronique des tissus autour des dents).
Les facteurs psychologiques sont parfois identifiés comme déclencheurs de la maladie ou de certaines poussées.
Dans 20 à 30 % des cas, on constate que la polyarthrite survient après un événement marquant ou « stressant », qu’il soit physique ou psychique (deuil, séparation, accouchement, intervention chirurgicale, etc.).
Comment se manifeste la polyarthrite rhumatoïde ?

Quand la PR est active, elle se manifeste par une inflammation articulaire avec des douleurs de rythme inflammatoire prédominant en fin de nuit, des réveils nocturnes, des gonflements et un dérouillage matinal de toutes les articulations, mais surtout les mains et les pieds.
Si l’inflammation persiste longtemps, l’articulation risque de s'abîmer et peut conduire à des difficultés dans la vie quotidienne.
L’évolution de la PR est variable selon les personnes et dépend du bon contrôle de l’inflammation. Si l’inflammation n’est pas bien contrôlée, cela peut conduire à des déformations articulaires ou à des complications qui font la sévérité de la PR.
La PR peut se manifester par de la fatigue et s’associe plus rarement à d’autres manifestations non articulaires, par exemple une sècheresse de la bouche et des yeux ou une atteinte pulmonaire .
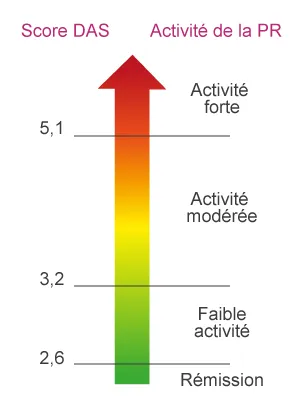
Une polyarthrite est active quand les patients rapportent des douleurs et des gonflements sur plusieurs articulations, avec sur les prises de sang, un syndrome inflammatoire. Les médecins utilisent un score d’activité (DAS, pour Disease Activity Score), qui permet de quantifier le degré d’activité.
légende : Représentation schématique des 28 articulations évaluées dans le DAS 28
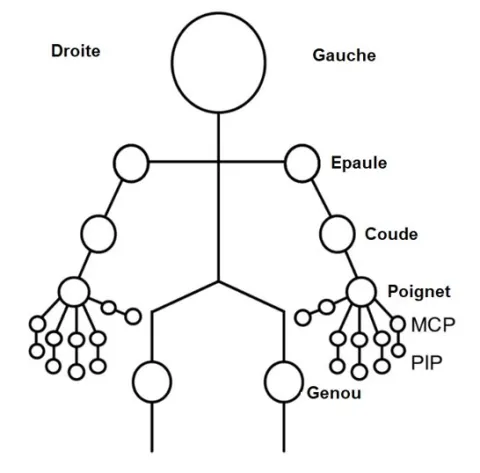
Le DAS prend en compte :
- le nombre d’articulations douloureuses (NAD),
- le nombre d’articulations gonflées (NAG),
- le syndrome inflammatoire (CRP ou VS),
- l’appréciation globale par le patient de sa maladie (EVA activité).
Les articulations examinées sont, le plus souvent, au nombre de 28 (cf. schéma).
La PR évolue par poussées inflammatoires intermittentes. Ces poussées sont variables en intensité et en durée. Le risque est de voir apparaître des complications suite à des poussées successives de la maladie. Les articulations s’abiment, et des difficultés dans les gestes de la vie courante peuvent apparaître.
Il est donc très important de contrôler l’inflammation, c’est-à-dire diminuer, voire arrêter l’inflammation des articulations.
Plus le traitement est débuté précocement (dans les premiers mois après le début de la PR) et adapté à l’activité de la maladie, plus les chances d’obtenir une rémission sont importantes.
légende : Echelle du Score DAS
Comment diagnostiquer une Polyarthrite Rhumatoïde ?
La PR est suspectée devant l’apparition de gonflements et de douleurs de plusieurs articulations. Devant ces signes, une consultation médicale est nécessaire pour effectuer des examens, affirmer le diagnostic et commencer un traitement adapté. Le rôle du rhumatologue est alors essentiel.
Le diagnostic repose sur des examens biologiques (des prises de sang qui montrent l’inflammation et la présence d’anticorps) et des examens d’imagerie ( échographie, radiographie). C’est la conjonction de ces différents arguments qui permet de diagnostiquer une polyarthrite rhumatoïde.
Le diagnostic est suspecté devant l’association de différents éléments :
- À l’examen : présence d’une polyarthrite touchant habituellement les mains et les pieds,
- À la prise de sang : un syndrome inflammatoire biologique (augmentation de la CRP (C réactive protéine) ou de la VS (vitesse de sédimentation) ) et la présence d'auto-anticorps qui sont des marqueurs de PR, comme le facteur rhumatoïde et les anticorps anti peptides cycliques citrullinés (anti CCP ou ACPA) )
- Sur les examens d’imagerie médicale des signes d’inflammation ou d’atteinte des articulations.(radiographies, échographie, Imagerie par résonance magnétique ou IRM)
Les anticorps anti-CCP ou ACPA sont très utiles pour le diagnostic de la PR car ils sont présents dès le début de la maladie et chez environ 70 % des patients. Ils sont beaucoup plus spécifiques de la maladie que les facteurs rhumatoïdes, c'est-à-dire que lorsqu’ils sont positifs, le risque d’avoir une PR est élevé. Il existe cependant des PR sans anticorps, qui sont dites « immuno-négatives ».
À la radiographie, les atteintes articulaires les plus précoces sont localisées au niveau des mains et des avant-pieds. Mais, ils ne faut pas attendre que les articulations soient lésées pour commencer les traitements de fond de la PR.
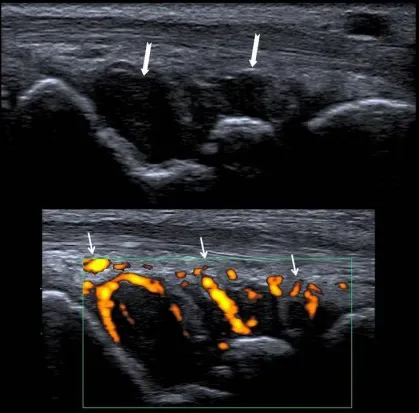
L’échographie permet de visualiser l’inflammation et les dégâts articulaires. Elle permet voir des signes d’inflammation et/ou les érosions qui ne se voient pas à l’examen clinique ou sur les radiographies. Ceci est très utile lors du diagnostic et aussi pour le suivi de la PR. L’IRM a les mêmes avantages que l’échographie mais elle est habituellement moins accessible.
Il existe des critères de classification de la PR qui orientent fortement vers le diagnostic et qui permettent de débuter un traitement.
Devant une polyarthrite débutante avec des radiographies normales et en l’absence d’un diagnostic d’une autre maladie :
Le diagnostic de PR est posé si le score est ≥ 6.
Comment se traite aujourd’hui la Polyarthrite Rhumatoïde ?

La prise en charge de PR doit être pluridisciplinaire, précoce et adaptée à l’inflammation . Elle a pour objectif de stopper l’évolution de la maladie, d’empêcher la destruction des articulations et de permettre la rémission.
Nous disposons de :
- Traitements symptomatiques de la douleur et de l’inflammation,
- Traitements de fond pour traiter stabiliser la maladie,
- Traitements locaux pour traiter une articulation douloureuse,
- Traitements non médicamenteux : réadaptation fonctionnelle/kinésithérapie personnalisée, auto-exercices, activité physique, soutien psychologique, aides sociales et professionnelle, éducation thérapeutique des patients (ETP).
Quelle est la stratégie thérapeutique devant une PR ?
La stratégie est définie par le rhumatologue en collaboration avec le médecin traitant.
Dans tous les cas, au début de la maladie et le plus tôt possible, l’important est de mettre en place un traitement de fond pour traiter la maladie générale et la stabiliser. Le premier traitement utilisé est en règle générale le méthotrexate, plus rarement le léflunomide ou la sulfasalazine.
Les traitements de fond ont un délai d’action retardé, qui peut mettre plusieurs semaines à apparaître (4 à 6 semaines). Des traitements symptomatiques pourront être prescrits en attendant leur efficacité. À terme, si le premier traitement de fond n’est pas suffisant, d’autres traitements peuvent être utilisés, comme les biothérapies ou traitements ciblés. Le suivi est très important, car il permet d’évaluer l’efficacité et la tolérance du traitement et de l’ajuster si nécessaire.
Les traitements médicamenteux de la PR
Les traitements symptomatiques :
Ce sont les antalgiques ou les anti-inflammatoires qui calment la douleur ou l’inflammation mais n’ont pas action sur l’évolution de la maladie.
Leur efficacité sur la douleur et l’inflammation se manifeste rapidement en quelques heures ou quelques jours et varie selon chaque patient, d’où la nécessité de trouver l’AINS qui est le plus efficace et le mieux toléré. L’horaire des prises est important pour obtenir une efficacité maximale au moment où les douleurs sont les plus importantes. Les effets indésirables principaux des AINS sont le risque d’ulcère gastrique, le risque d’hypertension artérielle ou d’insuffisance rénale.
Les corticoïdes sont utiles dans la PR, mais leur utilisation n’est pas forcément nécessaire. Lorsqu’ils sont nécessaires, ils sont prescrits au début de la maladie en attendant que les traitements de fond soient efficaces ou lors d’une poussée ou en cas de changement de traitement de fond. En raison de leurs effets indésirables, les corticoïdes sont arrêtés dès que possible ou maintenus à la dose la plus faible possible (quelques mg par jour).
Les traitements de fond de la PR
Les traitements de fond ont pour rôle d’arrêter ou de ralentir l’inflammation responsables de la progression de la maladie car il agissent en amont de l’inflammation. Ces traitements ont tous la particularité d’agir après quelques semaines voire au bout de 3 à 4 mois. Tous les traitements présentent de possibles effet indésirables qu’il faut connaître et surveiller, en particulier par une surveillance biologique
Le méthotrexate est le traitement de fond le plus utilisé et est administré en prise hebdomadaire en comprimés ou en injection sous-cutanée. Chez certains patients, en cas de contre-indication au Méthotrexate, le Léflunomide peut être prescrit. Il est administré en comprimés en prise journalière. Plus rarement, la Sulfasalazine est prescrite lorsque la PR est peu active, administrée en comprimés en prise journalière.
Les traitements de fond ciblés, biologiques (biothérapie ou biomédicaments) ou Jak-inhibiteurs, ont une bonne efficacité sur l’inflammation articulaire, sur la progression des lésions radiologiques et sont utilisées en cas d’inefficacité des traitements de fonds chimiques classiques, souvent en associations avec ces derniers.
Ils sont pris au long cours car la PR peut se réactiver lorsque ces traitements sont arrêtés.
Ils comprennent les biothérapies (biomédicaments) : anti-TNF alpha, Tocilizumab, l’Abatacept, Rituximab et les Jaki inbiteurs.
Quand utilise-t-on les traitements locaux ?
On utilise les traitements locaux lorsqu’une articulation reste douloureuse et /ou gonflée alors que le reste de la maladie est bien contrôlée. Il s’agit de l’injection dans l’articulation de produits cortisonés.
Les traitements non médicamenteux
- La rééducation et la kinésithérapie sont utiles lorsque les articulations sont lésées pour conserver ou améliorer la mobilité et la force. Le kinésithérapeute est chargé d’apprendre aux patients une auto-gymnastique à réaliser régulièrement à la maison. Le kinésithérapeute ou l’ergothérapeute donne aussi des conseils pour protéger les articulations, particulièrement en cas de poussées.
- L’activité physique régulière permet de garder une bonne mobilité et une bonne forme physique. Elle prévient aussi des complications cardiovasculaires.
- L’éducation thérapeutique (ETP) est importante dans cette maladie inflammatoire. Les programmes d’éducation thérapeutique permettent de mieux comprendre les mécanismes de la maladie, la place des traitements médicamenteux et non médicamenteux. Elle donne la possibilité aux patients de vivre une vie personnelle et sociale active avec leur maladie chronique et d’être plus autonomes. Les associations de patients proposent aussi des conseils et du soutien.
- Le soutien psychologique est parfois nécessaire car la maladie chronique peut s’accompagner d’anxiété, de stress voire de dépression.
- Une adaptation de poste de travail peut s’avérer utile pour garder une vie professionnelle satisfaisante.
- Cures thermales : elles peuvent être utiles, à distance d’une poussée inflammatoire. Elles ne remplacent pas l’activité physique régulière.
